水凝胶材料近年来在生物医药领域受到了广泛关注,例如作为药物递送载体、组织再生支架、外科手术缝合胶等。负载药物的水凝胶可在体内保持数日乃至数周的持续释放,很大程度上提高了药物的利用度和病人的耐受性,并降低药物毒副作用。如在水凝胶材料中引入酸、酶、光、热等刺激响应元件,则可进一步赋予水凝胶药物载体更加灵活可变的药物控制释放性能。近日,华东师范大学的程义云教授团队研发出一种可在43摄氏度的条件下快速降解的水凝胶,用于体内局部给药。这种水凝胶与光热材料结合,实现红外光(NIR)控制的药物按需递送。相关研究成果近期以A thermo-degradable hydrogel with light-tunable degradation and drug release为题发表在Biomaterials (2017, 112, 133-140)。

图1. 热降解水凝胶的制备方法以及热降解行为。
研究人员将偶氮类化合物改性成为两端为醛基的热降解交联剂(Thermo- degradable linker, TDL),与末端为氨基的四臂聚乙二醇交联形成水凝胶(图1)。该交联剂中的偶氮键可受热断裂,当温度上升到对应的化学键断裂温度时,凝胶的机械强度逐渐降低,呈现出热降解性能。其中由偶氮二异丁基咪唑啉改性得到的交联剂(TDL1)的热降解温度较低,大约在43摄氏度左右即可促发降解。在水凝胶中掺入光热纳米材料后,可通过近红外光来精确控制水凝胶中生物活性分子的释放。小鼠实验表明该水凝胶具有良好的生物相容性和体内稳定性,而近红外光的照射可促发水凝胶在体内快速降解,从而触发荧光探针、蛋白质、药物等分子的可控释放,有望实现药物的按需递送。该论文的第一作者为华东师范大学生命科学学院的胡婧婧博士。
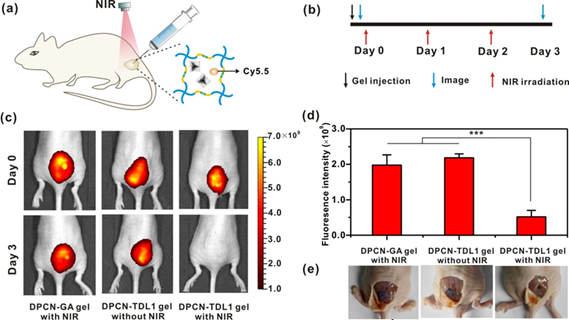
图2. 水凝胶在动物体内的光控热降解行为。近红外光可有效穿透小鼠皮肤和皮下组织,在局部产生热来促发水凝胶的降解和药物的释放。


